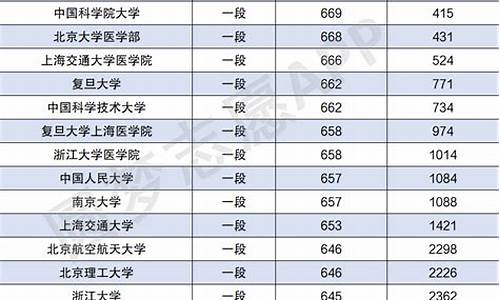
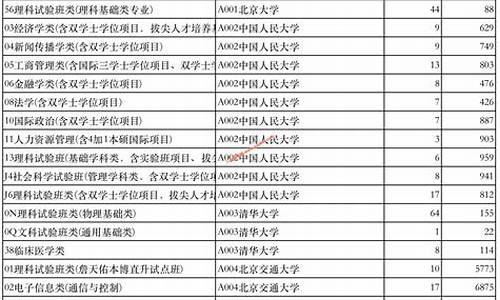
高考常见化学电子式_高考化学常考电子式
1.高一化学电子式怎么写,举例
2.高中化学
3.高中化学电子式
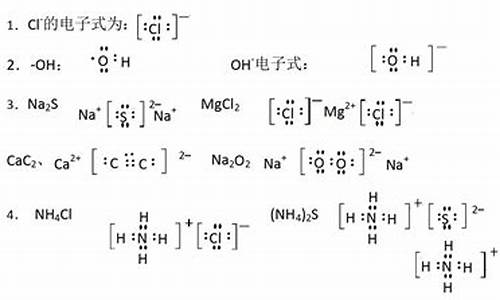
铁是单质,电子式与分子式相同,为Fe;氯气的电子式写法如下图:
原子依据元素的原子最外层电子个数的多少,先用小黑点“·”(或“×”)等符号在元素符号上、下、左、右各表示出1个电子,多余的电子配对。电子式单质分子必须正确地表示出共用电子对数,并满足每个原子的稳定结构。
扩展资料:
离子化合物电子式的书写规则口诀:多在外、少在内、小在外、大在内、阴阳相间。
1、多在外、少在内:同种离子数量多的放在离子式的最外侧,相对少一些的放在内侧书写。
2、小在外、大在内:对于不同价态的离子,也按其绝对值,遵照“大值在中间、小值在周边”的原则书写。
3、阴阳相间:书写时,要做到阴阳离子相间书写。
4、对于一种离子数明显多于其他离子的时候,也可以加角标表示,但较为少见。
高一化学电子式怎么写,举例
常见物质的电子式是硫化氢的电子式。
电子式是中学化学的常用化学用语。电子式是在元素符号周围用小黑点(·)或小圆圈(。)等表示原子最外层电子的式子。
因为主族元素的化学性质主要由元素原子的最外层电子数决定,电子式能反映原子间结合时电子共用和偏移关系,其书写又比原子结构示意图简单,表示的意义直观,还能反映原子间的实际连接顺序。搞好电子式的教学,有助于理解原子结构和物质结构知识,为结构式的学习打下基础。
电子式的书写应尊重客观事实。中学阶段常见简单粒子的电子式的书写,多数遵循使每个原子最外层达到8电子(或2电子)稳定结构的原则。少数不满足每个原子最外层达到8电子(或2电子)稳定结构,如PCl5、SO3及BeCl2、BF3等
用电子式可以表示原子、离子、分子、离子化合物、自由基等的结构,也可以用电子式表示分子、离子化合物的形成过程。如:
书写中应注意:
A.每个离子都要单独写,不能合并。
B.简单阳离子的电子式就是离子符号本身,阴离子、复杂阳离子必须加中括号并标明电荷。
C.不能将“?→?”写成“=”。
D.使用弧形箭头标明电子转移关系
E.共价化合物的形成过程中,不用弧形箭头,也不标中括号和离子的电荷。
高中化学
小小的纠正一下楼上……NaCl和CaCl2都是典型的离子化合物……何来共用电子对一说……NaCl的电子式是这样的:Na+[Cl]- 氯离子外有八个电子 打八个点点 其中有一个是来自于钠的这一个电子也可以写成× 以示区分离子化合物的电子式可以根据这个类推金属失去几个电子显几价 直接写就好非金属得到电子显负价 一般来说都是八电子饱和了然后那个括号把它括起来 表示它这八个电子中有一个或者多个是从别处得来的
高中化学电子式
在化学反应中,一般是原子的最外层电子数目发生变化。为了简便起见,化学中常在元素符号周围用小黑点“·”或小叉“×”来表示元素原子的最外层电子,相应的式子叫做电子式。
一、原子的电子式
原子的最外层有多少个电子就在其元素符号周围画多少个小黑点“·”或小叉“×”。原子的最外层电子有成对电子和单电子之别,写原子的电子式时,应使元素符号周围各个方向的电子尽量均匀分布。严格地讲,成对电子要排在同一个方位上,单电子分别排在不同的方位上。如锂原子写成·Li(或×Li)、氮原子写成·N·。
二、离子的电子式
阳离子 简单的阳离子(一般指单原子形成的阳离子)是元素原子失去最外层电子后形成的,此时若原最外层没有电子,其电子式就是它的离子符号,如钠离子写成Na+、钡离子写成Ba2+;复杂的阳离子是原子团失去一个或几个电子形成的,不仅要画出各原子的最外层电子以及它们的成键关系,而且要用“[ ]”将原子团括起来,并在其右上角标明所带的正电荷数,电子式中的小黑点和小叉总数为原子团中各原子最外层电子总数减去原子团所带的电荷数值。如铵根离子。
阴离子 简单阴离子,一般最外层是2个电子或8个电子的稳定结构,在元素符号周围画出最外层电子,并用“[ ]”将其括起来,并在右上角标明所带的负电荷数,其中小黑点和小叉总数为各原子的最外层电子总数加上所带的电荷数值的绝对值,如氯离子的电子式;复杂的阴离子,要根据各原子的成键关系画出所有原子的最外层电子,然后将它们括起来,并在右上角标明所带的负电荷数,其小黑点和小叉总数为原子团中各原子的最外层电子数之和加上所带的电荷数值的绝对值。如氢氧根离子。
三、单质分子的电子式
根据原子的最外层电子数和分子的组成判断出成键电子数和各原子的成键关系,再画出所有原子的最外层电子。如H2写成HH。
四、化合物的电子式
共价化合物 原子间通过共价键形成的化合物,原子间的单键即为一对共用电子,若为双键则有两对共用电子,依此类推。一般来说,8减去原子的最外层电子数等于该原子的成键数目(H、P例外)。写电子式时,共用电子对写在两成键原子之间,未成键的最外层电子,也应在元素符号周围画出。在共价化合物中,各元素原子最外层一般都达到了8电子(或2电子)的稳定结构。如HCl写成H 、H2O2写成H H。
离子化合物 由阴、阳离子的电子式组成,但相同的离子不能合并,若有多个阳离子或多个阴离子,书写时要使每一个离子都与带相反电荷的离子直接相邻,并注意对称、规范。。
五、游离基的电子式
游离基是由分子失去一个或多个原子所形成的活性基团,它显电中性,电子式中的小黑点和小叉总数为各原子的最外层电子数之和。如甲基的电子式为H C H,羟基的电子式为 H。
总的来说,就是均匀的在元素周围图小黑点,元素核外电子排列最外层是几,就画几个点
离子键的概念为阴、阳离子通过静电作用形成的化学键。以离子键结合的化合物叫离子化合物。
(离子化合物的是要标价态的)如下图:
共价键的概念为原子间通过共用电子对而形成的化学键。
由共价键形成的化合物是共价化合物。(共价化合物就是点小点的)如下图:
还有种混合起来的忘啥名了,长这样:
希望能帮到你吧,上图都是例子,
你说的下标是神马?_?(补充一下,最外层电子要稳定的话那些点的个数只能是2个或8个,2个一般是H因为它原本最外层电子是1个,要稳定就要与别的原子再给一个和他一起用才稳定,其他的最外层电子如果是第二周期4以下的失电子的也会变成2,其他的应该都是8了)
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。